Aus Emis.wiki
Karg (Diskussion | Beiträge) (→CRM) |
Karg (Diskussion | Beiträge) (→CRM) |
||
| Zeile 72: | Zeile 72: | ||
[[Image:8.png|400px|center]] | [[Image:8.png|400px|center]] | ||
| - | [[Image:9_new.png| | + | [[Image:9_new.png|300px|right]] |
1. Benannte Stelle Y, gültig bis XX.XX.XXXX (Dropdown-Menü, Einträge können in den emis.dienstprogrammen festgelegt werden (Gruppe "MDR Bekannte Stelle")). | 1. Benannte Stelle Y, gültig bis XX.XX.XXXX (Dropdown-Menü, Einträge können in den emis.dienstprogrammen festgelegt werden (Gruppe "MDR Bekannte Stelle")). | ||
Version vom 19. Mai 2021, 13:40 Uhr
Inhaltsverzeichnis |
emis.mdr ("Medical Device Regulation")
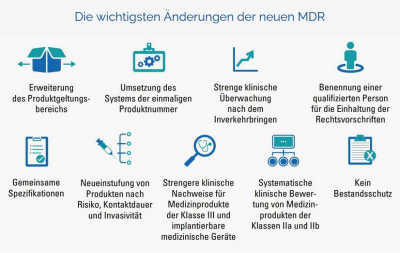
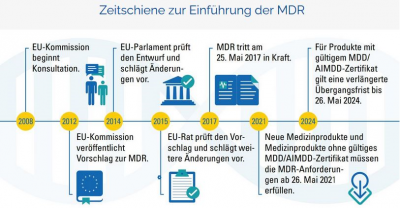
Mit dem emis.mdr-Modul sind Sie in der Lage die derzeit geltenden komplexen MDR-Anforderungen abzudecken. Dieses Modul wurde extra für unsere Kunden entwickelt, welche im medizinischen Bereich tätig sind. Im nachfolgenden Schaubild können Sie entnehmen, wie sich die Anforderungen im Laufe der Jahre verändert haben.
Damit Sie die ab dem 26.05.2021 die geltenden MDR Anforderungen für Medizin-Produkte usw. mit emis abdecken können, haben wir das Modul emis.mdr mit einer Vielzahl an Funktionen, welche die erforderlichen Qualitätsregularien abfragen, ausgestattet.
Artikelstamm
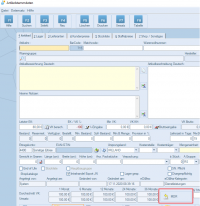
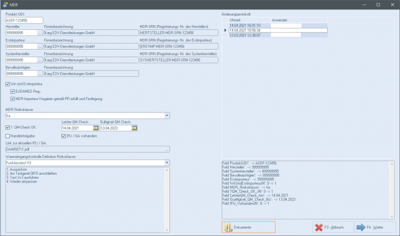
Im emis.artikelstamm können Sie mit dem Button "MDR" die MDR-Informationen zum Artikel aufrufen.In dieser Maske befinden sich folgende Informationen bzw. Funktionen:
- Produkt-UDI ("Unique Device Identification")
- Hersteller
- Bevollmächtigter
- Erstimporteur
- Wir sind Erstimporteur ja/ nein
- Wenn ja:
- EUDAMED ("Europäische Medizinproduktedatenbank") Reg. ja/ nein
- MDR-Importeur-Vorgaben gemäß PR erfüllt und Festlegung Labelung ja/ nein
- MDR-SRN (Registrierungsnr. des Herstellers, alphanumerisch)
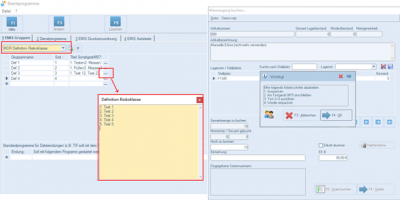
- MDR-Risikoklasse als Dropdown-Menü (Einträge können in den emis.dienstprogrammen festgelegt werden (Gruppe "MDR Risikoklasse")).
- uvm.
Wie wird definiert, ob das Produkt verkauft werden darf oder ob es gesperrt werden muss?
Dies erfolgt durch die Abfrage sämtlicher erforderlichen Qualitätsregularien, wie z. B.
- Gültigkeit (wenn überschritten, darf das Produkt nicht verkauft werden, das Produkt muss gesperrt werden).
- Handelsfreigabe ja/ nein
- IFU ("Instruction for use") vorhanden - ja/ nein
- Link zur aktuellen IFU (interner / und externer Link), Verknüpfung zur emis.dokumentenverwaltung.
- Wareneingangskontrolle Definition Risikoklasse.
Zu beachten ist hier, dass bei allen genannten Feldern, die Eingaben mit Datum und dem entsprechenden Anwender dokumentiert werden!
Sollten Eingaben auf aktiv gesetzt und somit die Kriterien nicht erfüllt sein, wird der Verkauf (Lieferscheindruck) gesperrt.
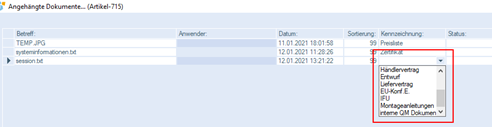
Außerdem können in der Dokumentenverwaltung zum Artikel folgende Dokumente abgelegt werden:
- EU-Konf.E.
- IFU
- Montageanleitungen
- interne Dokumente zum Qualitätsmanagement
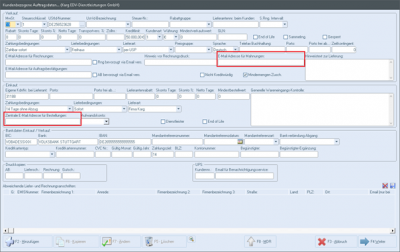
CRM
Folgende Felder wurden in den kundenbezogenen Auftragsdaten für emis.mdr hinzugefügt.
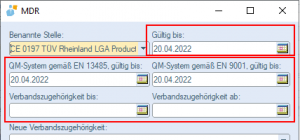
1. Benannte Stelle Y, gültig bis XX.XX.XXXX (Dropdown-Menü, Einträge können in den emis.dienstprogrammen festgelegt werden (Gruppe "MDR Bekannte Stelle")).
2. Die MDR Wiedervorlagen Benutzer und das Datumsfeld, lassen sich über die beiden Systemvariablen MDR_wv_user und MDR_wv_minus_x_tage festlegen
3. QM-System gemäß EN 13485, gültig bis XX.XX.XXXX
4. Die Automatische Wiedervorlage für einen Benutzer und für das Datumsfeld gemäß EN13485, kann durch die Systemvariablen EN13485_wv_user und EN13485_wv_minus_x_tage festgelegt werden.
5. QM-System gemäß EN 9001, gültig bis XX.XX.XXXX
6. Die Automatische Wiedervorlage für einen Benutzer und für das Datumsfeld gemäß EN9001, kann durch die Systemvariablen EN9001_wv_user und EN9001_wv_minus_x_tage festgelegt werden.
7. Verbandszugehörigkeit bis: (Datumsfeld mit automatischer Wiedervorlage (standardmäßig 14 Tage davor, kann in der Systemvariable "MDR_wv_minus_x_tage" festgelegt werden).
8. Verbandszugehörigkeit ab: (Datumsfeld mit automatischer Wiedervorlage (standardmäßig 14 Tage davor, kann in der Systemvariable "MDR_wv_minus_x_tage" festgelegt werden).
9. "Zentrale E-Mail PRRC:" Hier geht es um den Sicherheitsbeauftragter Medizinprodukte Hersteller
10. "Zentrale E-Mail BMS:" Hier geht es um den Sicherheitsbeauftragter Medizinprodukte Kunde
11. "Zentrale E-Mail QMB:"
12. MDR-SRN des Herstellers
13. MDR-SRN des Erstimporteurs
14. MDR-SRN des Systemherstellers
Bei den Punkten 6-8 wird jeweils automatisch ein einzelner Ansprechpartner im Kunden angelegt.
In den "_User" Systemvariablen muss der Anwender an den die Wiedervorlagen gesendet werden, mit Namen eingegeben werden (Wie im Personalstamm eingegeben wurde). Ist diese Systemvariable leer wird keine Wiedervorlage erstellt.
Bei den Datumsfeldern Systemvariablen "_minus_x_tage" muss eine Zahl eingegeben werden. Hierbei bedutet X = Tage vor Datum.
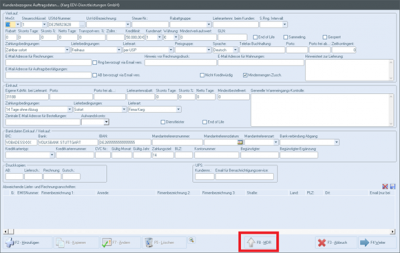
In den kundenbezogenen Auftragsdaten sehen Sie außerdem folgende Informationen:
- Im Bereich "Einkauf" wird eine zentrale Bestell-E-Mail-Adresse für den Lieferanten hinzugefügt
- Im Bereich "Verkauf" wird das Feld "Rechnung und Mahnung Mail-Adresse" geteilt, dass eine separate Mail-Adresse eingetragen werden kann.
Wichtig hierbei ist, wenn nur eine von Beiden ausgefüllt ist, wird automatisch diese E-Mail-Adresse verwendet. Wenn Beide ausgefüllt sind, wird dies bei der Rechnung und Mahnung unterschieden.
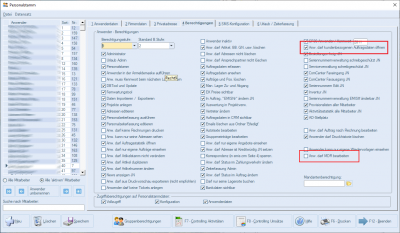
Personalstamm
Zudem finden Sie im emis.personalstamm das Recht, ob ein Benutzer die kundenbezogenen Auftragsdaten im emis.crm öffnen darf oder nicht. Ebenfalls finden Sie hier das Recht, ob ein Benutzer das Recht hat, das MDR zu öffnen.
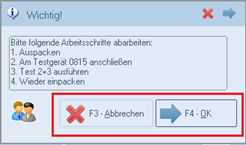
Bestell und CP30
Zusätzlich wurde das emis.bestellmodul, sowie emis.cp30 um die MDR-Risikoklasse erweitert, dass, wenn die Meldung erscheint, man mit "OK" und "Abbrechen" bestätigen kann.
• Bei "OK" wird im Artikel ein Eintrag im MDR-Protokoll hinzugefügt.
• Bei "Abbruch" wird die Buchung der Position im Bestellmodul abgebrochen, bzw. im CP30 der Wareneingang für diese Position.